

Zellfreie Implantate
Historie
Zellfreie Implantate gibt es seit der zweiten Generation der ACT, nämlich seit 1998.*
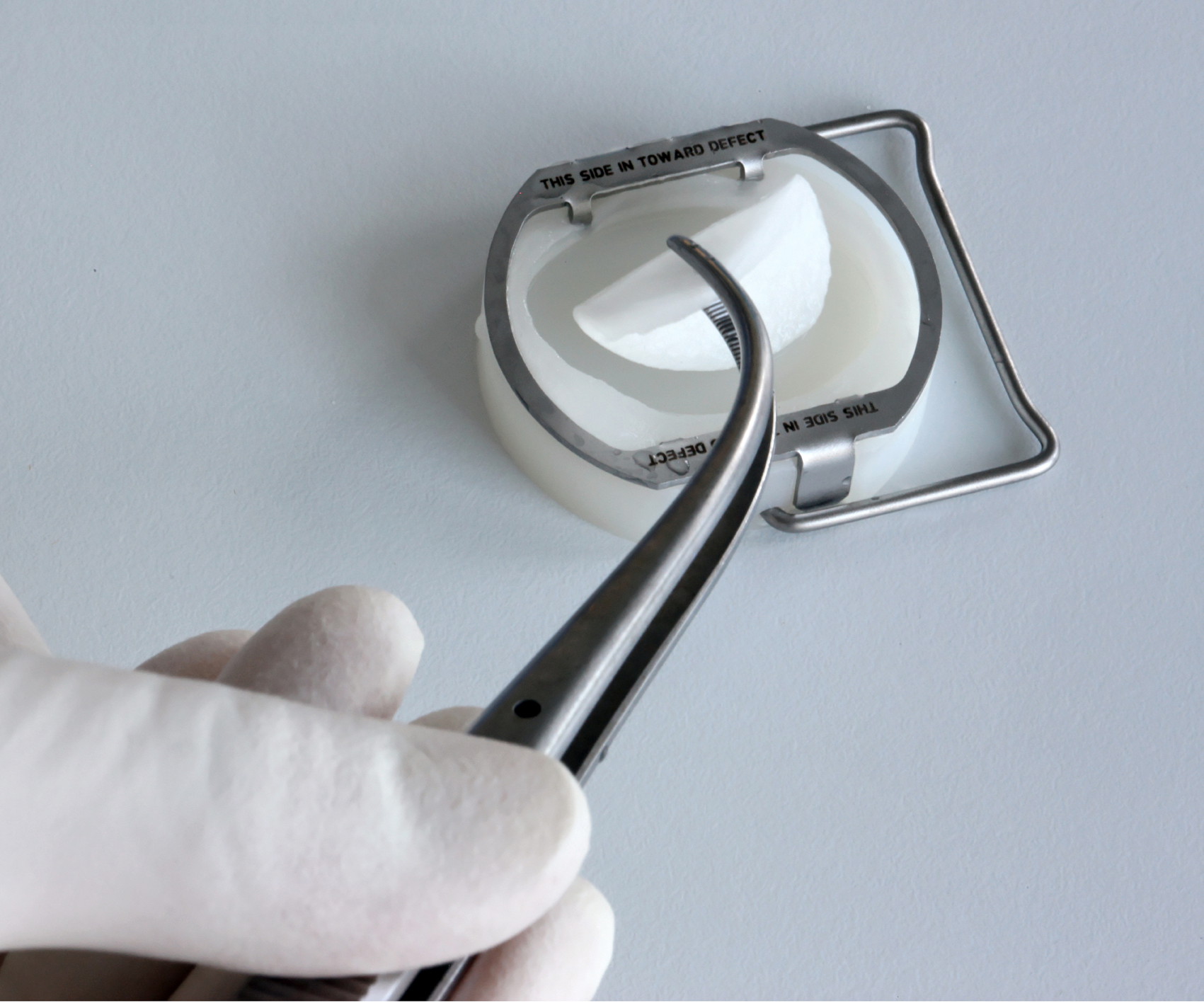
Bei der ersten, der Chondrogide-Membrane, handelt es sich um eine biphasische Kollagen I-III Matrix, die zunächst dazu diente, die gezüchtete Knorpel-Zellsuspension wasserdicht abzudecken, sodass man auf das zusätzliche Trauma und die Schwierigkeiten mit der Präparation eines Periostlappens verzichten konnte. Diese Chondro-Gide© Membran ist natürlich resorbierbar und kann geklebt und genäht werden.
Seit 2003 wird die Chondro-Gide® Membran für die „AMIC®“ (Autologe matrix induzierte Chondrogenese) angeboten. Der Gedanke der dahinter steckt ist, die bei der Mikrofrakturierung freigesetzten Knochenmarkzellen im Defekt zu behalten und zur Knorpelregeneration beizutragen, da doch sonst viele Zellen aus dem Defekt bedeckenden Gerinnsel verloren gehen können.
Tatsächlich zeigen Mittel und Langzeitstudien, dass die klinischen Ergebnisse der reinen Mikrofrakturierung deutlich schlechter ausfallen, als die der AMIC*. Auch die histologischen Ergebnisse sind besser als die der Mikrofrakturierung.**
Wegen der hohen Anzahl an intraläsionalen Osteophyten und subchondralen Zysten für die Mikrofrakturierung – in 20%-50%*** entstehen intralesionale Osteophyten, mit etwas geringerer Ausprägung für die AMIC®.
Durch die NAMIC® (Nanofrakturierung + AMIC) wurde versucht, den knöchernen Defekt soweit zu verkleinern, dass diese Komplikationen weiter reduziert werden sollten.
CaRes 1S®, eine Kollagen I Membran, war 2009 das erste zellfreie Implantat, das nach Chondro-Gide® die CE Zulassung Medizinprodukt Klasse III erhielt.
Hyalofast® war das nächste zellfreie Produkt, das zunächst als Hyalofast C© mit kultivierten Knorpelzellen beladen auf den Markt kam und seit 20xx als zellfreie Matrix angewendet wird.
Eigenschaften von zellfreien membranen
- Hyaluronsäure und Kollagen I und I-III über lange Zeiträume als Matrices bewährt
- Zellfreien Implantate sind in der Lage die Reifung und Integration der Zellen zu fördern.**
- Aber, für gutes hyalin-ähnliches Regenerat benötigt man Zellen!*** 4* Zellen, als kultivierte Knorpelzellen, Minced Cartilage, Mikrofrakturierung usw.
- Zellfreie Implantate können für nahezu alle chondralen u. osteochondralen Defekte bis 6-8mm Tiefe zum Einsatz kommen.5*
- Chondrozyten können durch Proteolyse Barrieren überwinden sich amöboid bewegen und so Kollagenmatrices und einige andere Matrices besiedeln.*
- Stimuliert werden sie hierzu durch diverse chemotaktische Substanzen, u.a. durch mesenchymale Progenitorzellen im Knorpelgewebe.** ***
- Die migrierenden Chondrozyten produzieren Kollagen II, sodass es sich um voll differenzierte Chondrozyten handeln muss.****
- Es gibt heute viele Optionen, uneinheitliches Vorgehen hinsichtlich Fixation und Präparation des subchondralen Knochens
- Auch die Lagerung ist sehr unterschiedlich (gekühlt/eingefroren/Raumtemperatur)
studienlage
- Es gibt viel versprechende 5 Jahresergebnisse für CaReS 1S ®5*, Chondrotissue ®**, BST-CarGel®4* , Maio-Regen ®***,Hyalofast®7* und Chondro-Gide®6*
- wobei Chondro-Gide® die mit Abstand umfangreichste Literatur mit den längsten Nachuntersuchungszeiten aufweisen kann.
- Zur AMIC gibt es eine Langzeitstudie 8* und 6 Studien mit mittlerer Nachuntersuchungszeit *-6*
- 1 Level II* und 6 Level IV Studien
- AMIC® ist in allen 5-9 Jahresstudien mit 75-87% Zufriedenheit der Mikrofrakturierung signifikant überlegen.*
- Auch größere Defekte (2-8cm²) scheinen von der AMIC®* profitieren von 7* , aber 30% Osteophyten**
Zukunft
Neueste Entwicklung sind Zellfreie Implantate aus dem 3D-Drucker. Sie besitzen die einzigartige Fähigkeit die verschiedenen Techniken matrix-basiert, zellfreie Matrix durch in situ 3D Bio-Printing eine Replikation anatomischer Strukturen, biologische Funktionen und mechanische Eigenschaften des originären Knorpels nachzubilden und im Besonderen die zonale Differenzierung des Knorpels in oberflächliche, mittlere und tiefe Zone zu rekonstruieren.
indikationen und Kontraindikationen
- Ergebnisse sprechen für zellfreie Implantate ggf.in Kombination mit Zellen für Defekte
- bei ganz kleinen Defekten, kleiner 2 cm², können Chondrozyten aus dem gesunden Umgebungsknorpel ggf. in den Defekt einwandern und ein Knorpelregenrat bilden.
- bei größeren Defekten ist die Gabe von Zellen, Knorpel oder „Stammzellen“ erforderlich.
- Zur Zeit besteht die Indikation für zellfreie Implantate eher für kleinere Defekte von 2-4 cm²
- Zellfreie Implantate können für nahezu alle kleineren chondralen u. osteochondralen Defekte zum Einsatz kommen.*
- Wie auch alle anderen knorpelregenerativen Verfahren verändern die Osteoarthrosegrade 2-4 das Ergebnis ganz wesentlich negativ*
- Aber auch das Patientenalter, Ursache und Größe der Läsion sind das Ergebnis beeinflussende Faktoren*
Aktuell auf dem Markt befindliche zellfreie implantate
- Agili-C©: CartiHeal (Israel)
- BST-CarGel®, Primal Enterprises Limited, Canada, Chitosanlösung
- CaRes 1S®, Arthro Kinetics AG, Germany, Kollagen Typ I vom Rattenschwanz
- Cartimaix®, Matricel GmbH, Deutschland, Schweinekollagenmembran
- Chondrofiller® liquid, Meidrix Biomedicals GmbH, Deutschland, Kollagen Typ I vom Rattenschwanz.
- Chondro-Gide®, Geistlich Pharma, Switzerland, Schweinekollagen Typ I/III
- Chondrotissue®, BioTissue Technologies GmbH, Switzerland Polyglycolic acid fleece und freeze-dried sodium hyaluronate
- Coltrix®, Innotec Healthcare, Südkorea, Typ-I-Atelo-Kollagen vom Schwein
- Gelrin C®, Regentis Biomaterials Ltd., Israel, Hydrogel of polyethylene glycol (PEG-DA) und denaturiertes Fibrinogen
- Hyalofast®, Anika Therapeutics, Inc., USA, Biodegradables Hyaluronan (HYAFF1)
- Maioregen®, TM Fin-Ceramica Faenza S.p.A., Italy, Deantigenated Typ I Pferdekollagen
- MeRG®, Bioteck S.p.A., Italy, Microfibrilläre Kollagenmembran
- Novocart Basic®, TETEC, biphasische Kollagenmembran
fazit aus sicht des qkg
- Bei Defekten bis 1-2 cm² können Matrices ohne zusätzliche Zellen verwendet werden
- Bei Defekten bis 4 cm² sollten zusätzlich zur Matrix-Verwendung Zellen akquiriert werden
- mittels Nanofrakturierung (die Mikrofrakturierung sollte verlassen werden), oder besser noch
- mittels minced Cartilage, da hier die subchondrale Knochenlamelle nicht beschädigt wird.
- mittels Knochenmarkaspirat mit z.b. Yamshidinadel, was aber aktuell „off Label“ erscheint, obwohl hierbei die gleichen Knochenmarkzellen verwendet werden, die man auch bei den knochenmark-stimulierenden Verfahren – Abrasion, Mikrofrakturierung und Nanofrakturierung – gewinnen möchte.
- Defekte größer als 4 cm² sollten mit einer MACT versorgt werden
Alle Informationen zur den beschriebenen Verfahren sind Evidenz basiert. Mehr Details, Bildmaterial und Videos zu den einzelnen Techniken, sowie Literaturquellen können QKG-Mitglieder in unserem Knorpelforum einsehen. Werden Sie Mitglied!

